美国的研究者在小鼠前列腺癌移植瘤模型上,利用蛋白质组+磷酸化蛋白质组揭示了前列腺特异性膜抗原靶向放射性配体疗法(PSMA RLT)治疗引起的蛋白质组和磷酸化蛋白质组分子改变,并为寻找潜在的治疗抗性机制提供了前期数据积累。研究成果以“Mechanisms of Resistance to Prostate-Specific Membrane Antigen–Targeted Radioligand Therapy in a Mouse Model of Prostate Cancer”为题,发表在 Journal of Nuclear Medicine(IF:11.082)上。

研究结果
1. PSMA RLT(前列腺特异性膜抗原靶向放射性配体疗法)在小鼠前列腺癌移植瘤模型上的治疗效果
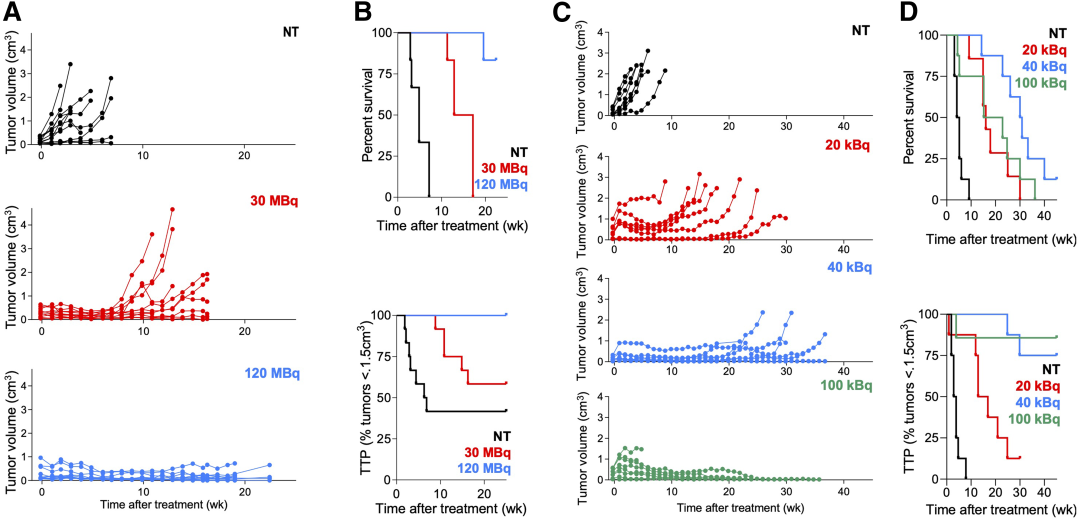
研究者分别使用以下两种不同的PSMA RLT对前列腺癌移植瘤小鼠进行治疗,并通过检测小鼠体重、肿瘤体积、进展到最大肿瘤体积一半的时间(TTP)、生存情况等记录治疗效果。
| PSMA RLT疗法 | 说明 | 治疗剂量 |
| [177Lu]Lu-PSMA-617 | 释放β粒子 | NT(未治疗)、30MBq、120MBq |
| [225Ac]Ac-PSMA-617 | 释放α粒子 | NT(未治疗)、20kBq、40kBq、100kBq |
结果显示,两种不同的PSMA RLT疗法可以诱导显著的、剂量依赖的肿瘤减小以及增加的TPP和总生存。其中,[177Lu]Lu-PSMA-617 100kBq有最佳控制肿瘤效果,但产生了一定的毒性。接下来,研究者选择了[177Lu]Lu-PSMA-617 30MBq和[225Ac]Ac-PSMA-617 40kBq的治疗活性进行比较,因为它们在能量沉积等方面具有可比性。[225Ac]Ac-PSMA-617 40kBq有更长的生存期。
【补充知识】:
靶向放射性配体疗法(RLT)的作用机理是将治疗性放射性同位素(放射性粒子)与能靶向结合肿瘤特异性分子的配体连接在一起。注入血液后,配体与特异性靶向的肿瘤细胞结合,从而让放射性粒子产生的放射线能集中对局部的肿瘤细胞进行杀伤,减少对周围和全身其它健康组织的损伤。
2. PSMA RLT疗法诱导DNA损伤反应/复制应激反应、细胞周期阻滞和TP53信号激活
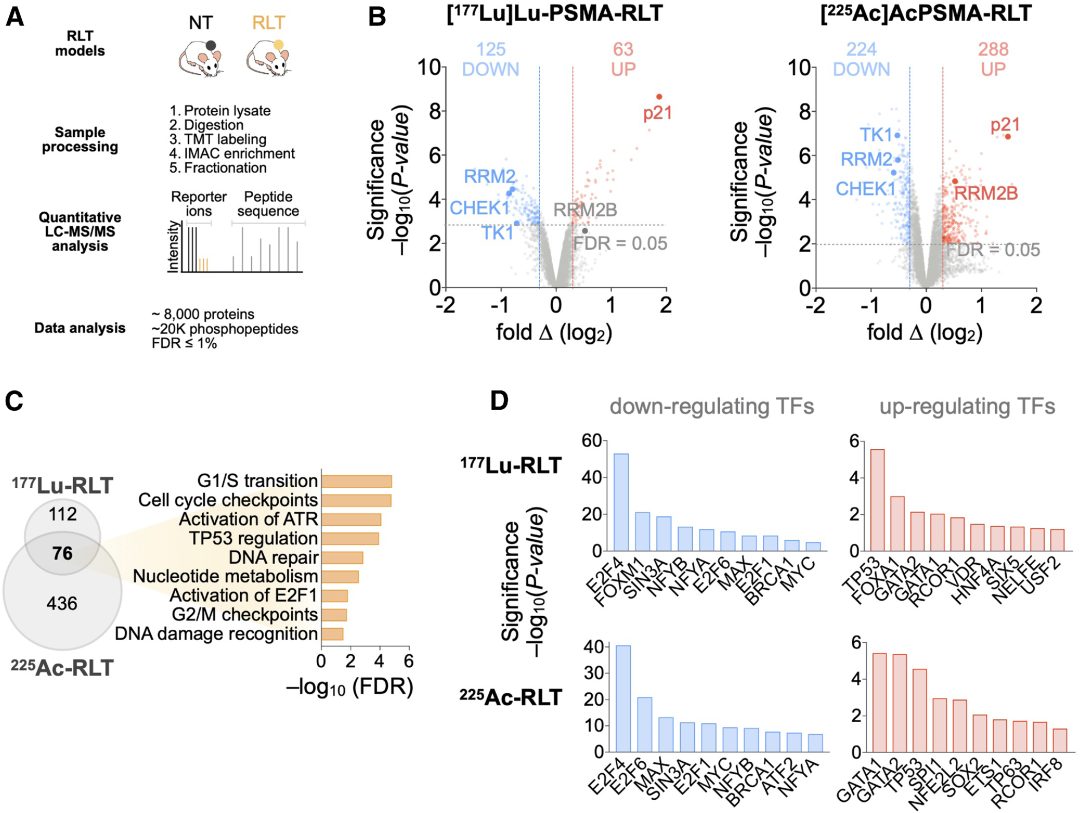
为了探索PSMA RLT治疗诱导的肿瘤分子改变,研究者对未进行RLT治疗和治疗的小鼠移植瘤进行了蛋白质组+磷酸化蛋白质组检测(3-5个生物学重复)。[225Ac]Ac-PSMA RLT治疗后,分别在蛋白质组和磷酸化蛋白质组上产生了3.3%和2.8%的改变。[177Lu]Lu-PSMA RLT治疗后,在蛋白质组和磷酸化蛋白质组上产生了2.5%的改变。因为两种治疗方法的差异,所以产生的分子变化也存在差异。研究者对差异蛋白的共有富集GO功能进行分析,发现DNA损伤反应/复制应激反应(DDR/RSR)和细胞周期阻滞是最受到影响的功能条目。此外,RLT疗法还造成了响应基因毒性应激和细胞周期进展的转录因子(TF)GATA1和REST 共抑制因子1的上调,以及BRCA1、MYC和E2F家族成员的下调。
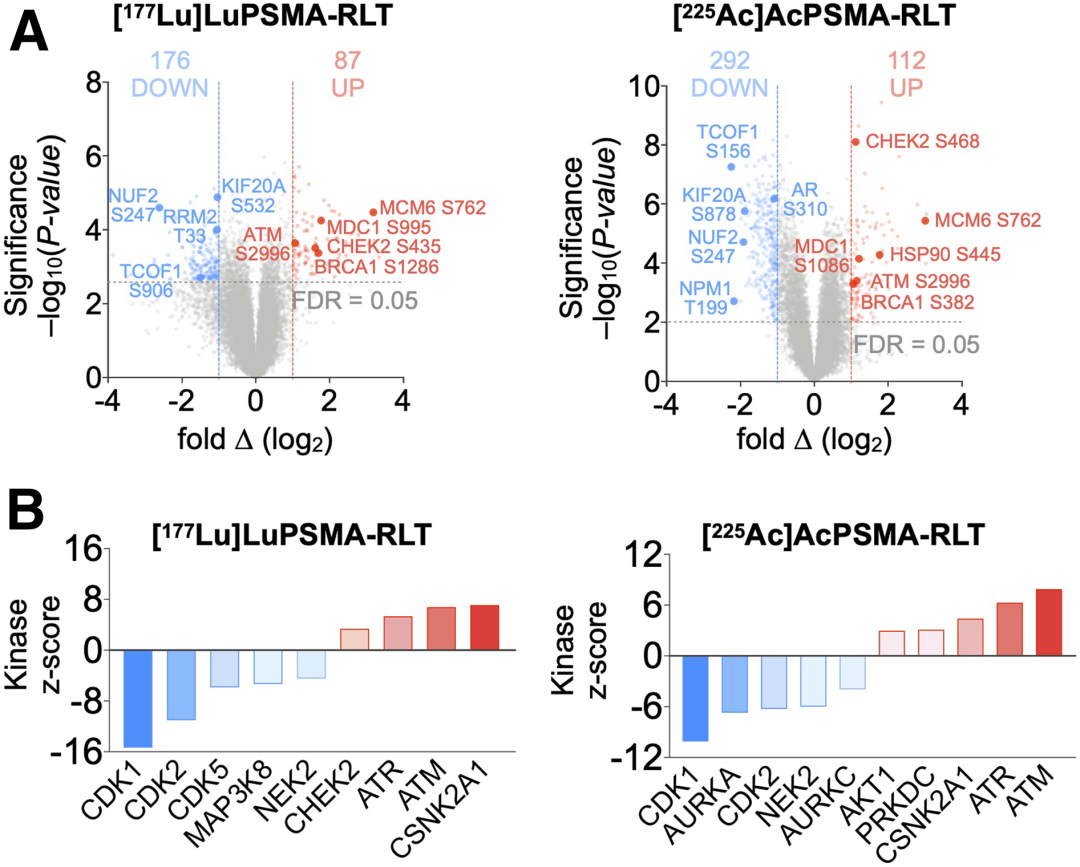
激酶-底物富集分析(KSEA)显示,RLT治疗通过上调ATM在Ser2996的磷酸化及已知的ATM、ATR和CSNK2A1底物(如BRCA1)的磷酸化和抑制细胞周期蛋白依赖激酶的底物(如核糖核酸还原酶调节亚基M2和RRM2)的磷酸化增强了ATM、ATR和酪蛋白激酶2A.1(CSNK2A1)的激酶活性。
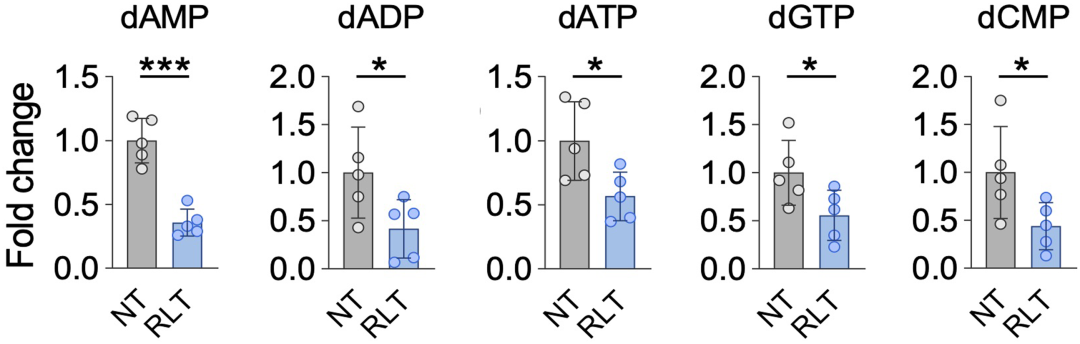
在共有GO功能条目中有“核苷酸代谢”条目的富集,研究者对dAMP、dADP、dATP、dGTP和dCMP的含量进行检测,这些核苷酸在RLT治疗后均显著下调,印证了核苷酸代谢的改变以及复制应激的存在。
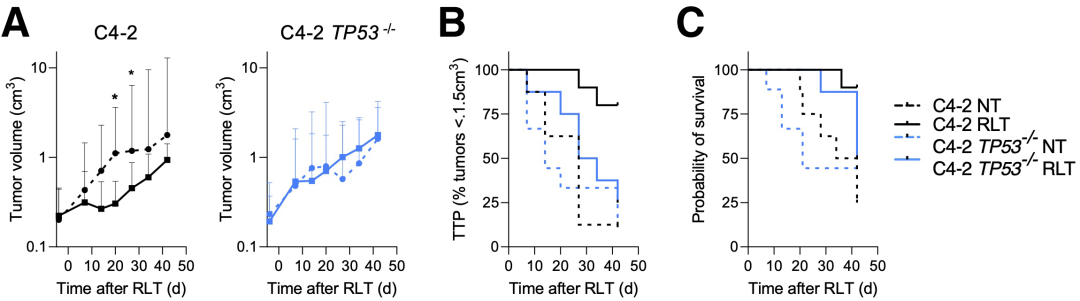
3. TP53缺失诱导肿瘤对PSMA RLT响应的减弱
TP53调控是前述共有的GO功能富集条目之一,通过文献调研也表明,TP53改变是转移性前列腺癌中最常见的突变,且与辐射抗性相关。因此研究者检测了TP53改变对前列腺癌响应RLT的影响。研究者分别构建了TP53野生型和TP53-/-的C4-2移植瘤小鼠模型,并进行PSMA RLT治疗。结果显示,与野生型TP53组相比,TP53-/-移植瘤组对RLT响应减弱。
研究总结
研究者在小鼠前列腺癌移植瘤模型上检测了PMSA RLT治疗的效果和相关分子改变。研究表明,两种PMSA RLT均能有效抑制移植瘤生长。PMSA RLT治疗和未治疗的移植瘤蛋白质组学和磷酸化蛋白质组比较揭示了相关的分子改变。两种治疗手段产生的分子改变显著富集在DNA损伤反应/复制应激响应及细胞周期阻滞相关功能,且均导致一些激酶活性的上调,如ATM、ATR和酪蛋白激酶2A.1(CSNK2A1)。最后,考虑到TP53调控在两组学中的显著富集以及其被报道与辐射抗性相关,研究者检测了TP53缺失条件下,移植瘤小鼠对RLT的响应。结果表明,TP53缺失将导致移植瘤小鼠对RLT响应的减弱。总体,本研究为了解PMSA RLT引起的分子改变和可能的治疗抗性机制提供了宝贵的数据。
蛋白质组学+磷酸化蛋白质组学实验方案建议
蛋白质组学是一种高通量检测技术,可获得大量基因在蛋白质水平的表达数据。基于差异分析可为后续的研究提供更明确、可靠的一些方向。蛋白质组学研究的是蛋白表达,磷酸化蛋白质组学研究的是蛋白的修饰,两组学联合能解释蛋白不同层面的信息,逻辑严谨,互为补充,为识别研究课题相关的磷酸化事件、关键信号通路和分子机制提供了一个全面的视角,有助于发表高水平研究。
吉凯基因可提供蛋白质组、磷酸化蛋白质组及激酶-底物富集分析(KSEA)等技术服务,并基于对大量文献的梳理,整理了一套蛋白质组学+磷酸化蛋白质组学的实验方案设计和写作思路,欢迎前来咨询。

完整的蛋白质组+磷酸化蛋白质组的产品资料,请联系吉凯当地销售工程师或拨打电话4006210302。
吉凯基因凭借多年在靶标筛选及验证服务领域的技术积累,建立的标准化 、工程化 、系统化的GRP平台,为中国研究型医生提供科研服务,加快科研成果转化。其中,多组学平台包含蛋白质组学平台和高通量测序平台:
·蛋白质组学平台拥有多台timsTOF Pro、Exploris 480高精度质谱仪,专业的Spectronaut Plusar、Mascot等分析软件,提供专业的4D、DIA、TMT、PRM、磷酸化修饰组、olink蛋白质组等检测服务,强大的机器学习算法、IPA分析、蛋白基因组分析服务,系统的生物标志物、分子分型、药物靶点、基因功能研究等解决方案,真正让广大研究型医生的科研工作更省心、更省力、更高效;
·高通量测序平台分为常规测序服务和单细胞测序服务:单细胞测序拥有10x和BD两个平台,提供单细胞RNA-seq、单细胞核测序、单细胞混样RNA-seq、单细胞TCR/BCR、单细胞(RNA+ATAC)、空间转录组测序等服务;常规测序服务提供meRIP-seq(m6A/m1A/m7G/m5C 等RNA甲基化修饰测序)、acRIP-seq(ac4C RNA乙酰化修饰测序)、ATAC-seq、Ribo-seq(翻译组测序) 、mRNA/miRNA/LncRNA/circRNA-seq、全转录组测序(两文库/三文库)、外泌体miRNA/LncRNA-seq、WGS/WES、WGBS、RRBS、BSAS等服务。
