Dual-Luciferase双萤光素酶报告基因检测系统在细胞中同时表达萤火虫萤光素酶和海肾萤光素酶,两者没有种属同源性并对应不同的反应底物,故而没有交叉干扰。以Luciferase为核心,构建研究对象到相应位置,转染细胞,裂解细胞,分别加荧光素酶底物,用荧光测定仪检测荧光强度,通过数据得出基因表达量,从而确定构建序列的功能。双报告基因则通过共转染的“对照”作为内参为试验提供一基准线,从而可以减小细胞活性和转染效率等外在因素对实验的影响,使得数据结果更为可信。
双荧光素酶实验往往不会单独出现在文章中,而是在验证结合位点时,作为点睛之笔,拔高整片文章的上限。本文结合吉凯基因的客户文献,与老师们一同回顾下双荧光素酶实验的两大经典应用。

本片文献中介绍道:葡萄糖刺激胰岛素分泌受损(GSIS)是2型糖尿病的一个标志。胰岛B细胞KLB基因的敲除,导致GSIS缺陷和葡萄糖耐受不良,而AAV介导KLB基因的修复,可缓解2型糖尿病小鼠胰岛GSIS缺陷。在接下来的机制验证环节,作者锁定了KLB-STAT3-HIFα通路,那么转录因子STAT3具体结合上HIFα启动子上哪段序列来发挥作用呢?
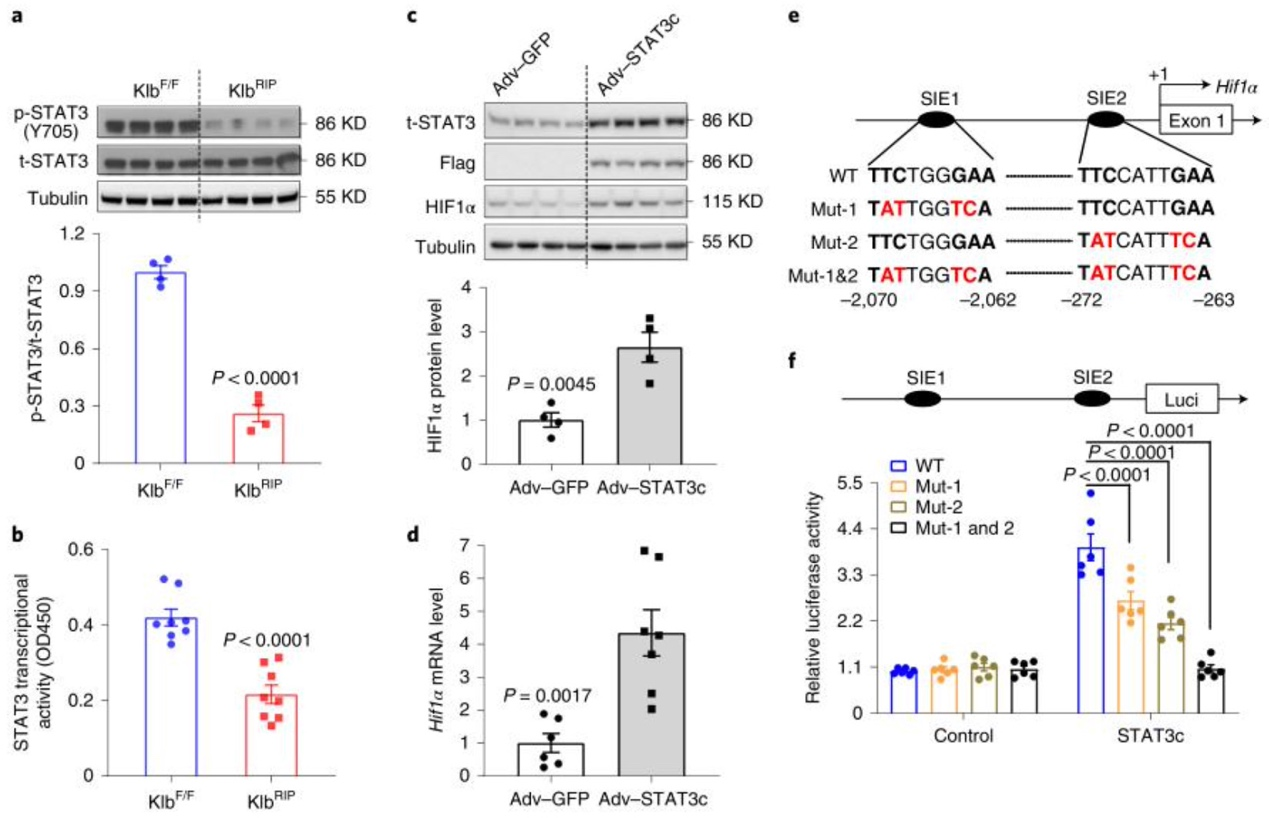
为了验证这一猜想(Fig e-f):作者在网站中,预测了STAT3在HIFα启动子上的两处结合位点(WT型),并且构建了3个突变质粒,分别为仅突变位点1的Mut-1、仅突变位点2的Mut-2,与同时突变位点1 + 位点2的Mut-1&2。双荧光素酶结果显示:Mut-1与Mut-2的相对荧光值均下降,但Mut-1&2的相对荧光值下降幅度最大,说明预测的两处结合位点均为STAT3在HIFα启动子上的有效靶点。如果老师们不太了解转录因子-启动子的操作方法,可以点击下方链接(https://mp.weixin.qq.com/s/CMwNob4kI8d7rBPlQEaKWA),观看我们吉凯病毒构建组的陈博录制的操作视频,聪明的小伙伴肯定一学就会。

本文探索了miRNA-22-3p在阿尔兹海默病(AD)中的功能和作用机制。体外实验中,过表达miRNA-22-3p可显著改善小鼠海马神经元细胞系HT22细胞的凋亡;体内实验过表达miRNA-22-3p,可改善阿尔兹海默病模型小鼠的认知功能、减轻β淀粉样蛋白(Aβ)沉积。在蛋白组学分析,锁定了差异蛋白SOX9,进一步通过GO和KEGG分析,挑选了NF-κB信号通路。那么miRNA-22-3p是结合上了SOX9的哪段序列,来发挥抑制作用的呢?

首先作者通过网站预测出miRNA-22-3p在SOX9中的结合位点,结果显示:miR-22-3p和Sox9的最低自由能为−21.0 kcal/mol,22个碱基中有17个位点相结合(Fig A)。双荧光素酶实验进一步证实了miR- 22-3p与Sox9的结合关系。结果显示,向野生Sox9组添加miR-22-3p会导致荧光显著降低,但在突变Sox9组中没有降低(Fig B)。
三、Lentivirus-CMV-Luciferase活体成像[4]
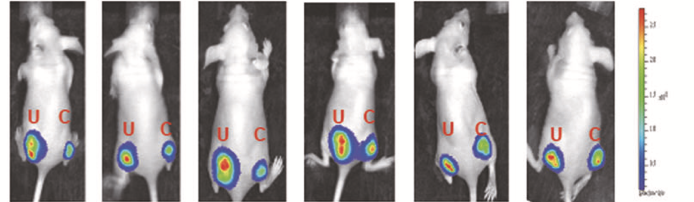
四、分析信号通路是否激活[5]
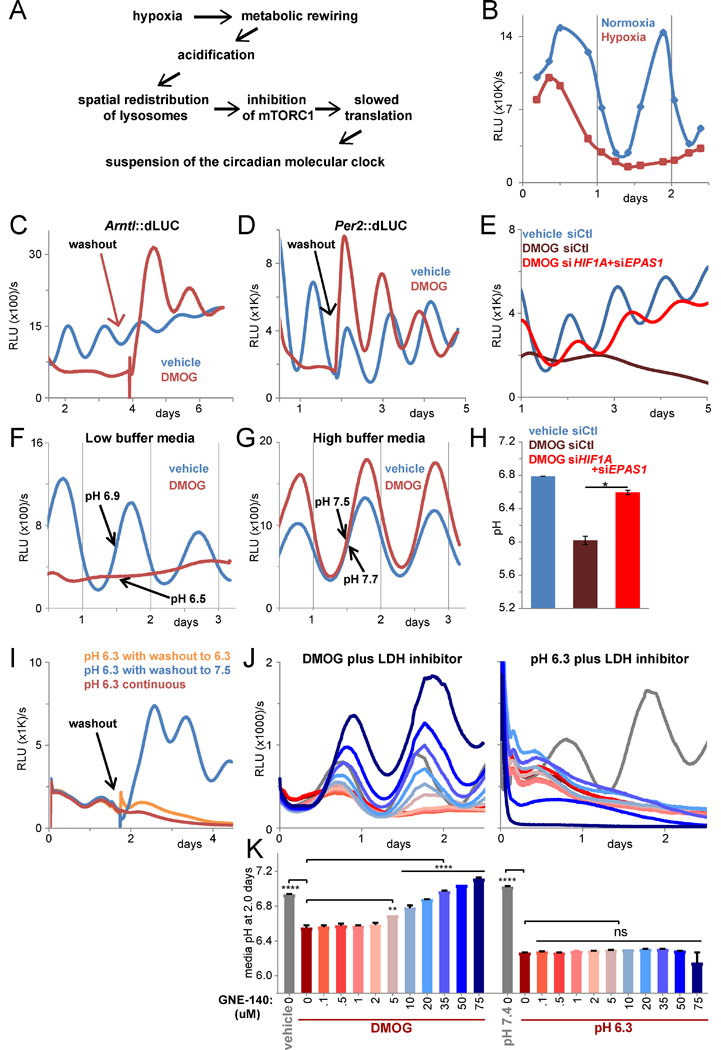
将该信号通路的下游响应原件序列构建入报告基因载体,在不同上游信号条件下,荧光素酶活性代表了通路的下游响应。比如说,将HIF1α的响应原件hypoxia-responsive element (HRE)插入luciferase报告载体(pGL4质粒图谱)构建稳转细胞株,可以用于低氧相关通路的研究。
作者的实验流程图如Fig A,Fig B-K:通过低氧产生的酸性环境,来调节培养体系的pH;加入HIFα的siRNA或LDH抑制剂,观察下游通路的响应程度,而观察的方法就是通过算出双荧光素酶荧光强度的比值,来统计结果的。
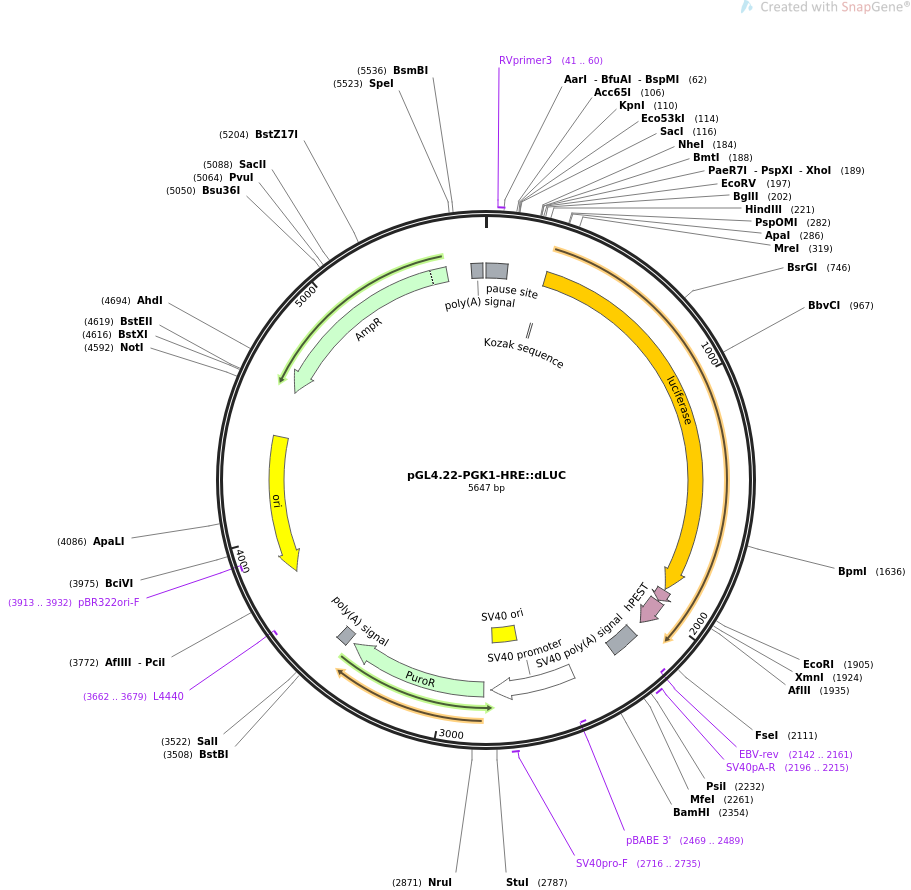
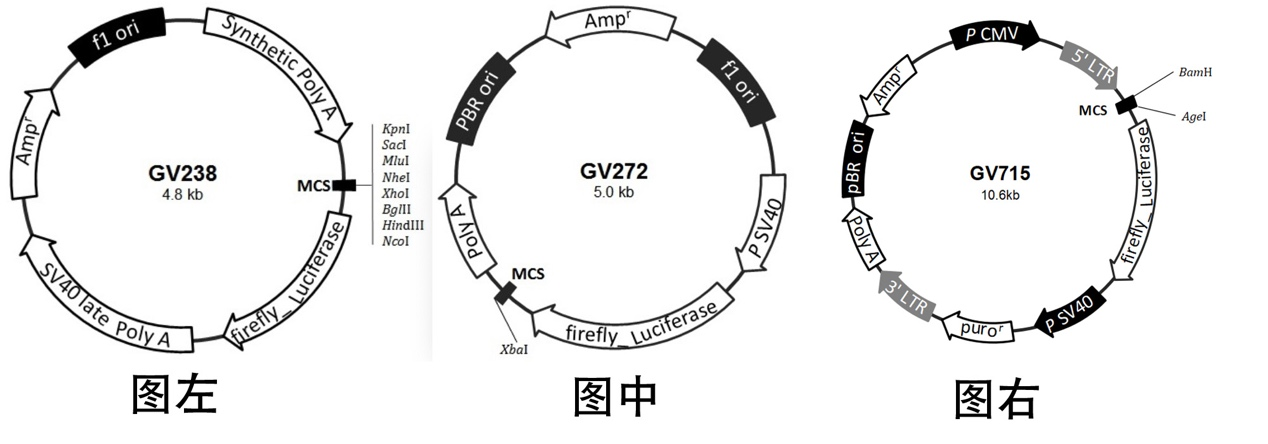
最后,做转录因子-启动子预测实验,我为老师推荐GV238载体(下图左),默认取基因转录起始位点上游2K序列构建报告系统;做miRNA-靶基因结合实验,我为老师推荐GV272载体(下图中),靶基因选择为miRNA结合位点两端各延伸100bp,构建报告系统。随着研究的深入,如果pGL3质粒转染工具细胞(293T细胞)无法满足实验需求,例如老师想要在目的细胞(血液细胞)中,表达荧光素酶,这是推荐老师选用慢病毒(下图右)作为载体GV715[6]。

公众号底部菜单栏【新功能】上线!
病毒实验帮
免费在线学习《国自然热点研究》、《数据库及软件操作教程》
一键下载《病毒使用手册》、《高分文献》
还有不定时的送新书、抽奖活动,赶紧来扫码关注一波吧
参考文献
1. Liu Y, Wang J, Shou Y, Xu W, Huang Z, Xu J, Chen K, Liu J, Liu D, Liang H, Yang H, Zhang X. Restoring the epigenetically silenced lncRNA COL18A1-AS1 represses ccRCC progression by lipid browning via miR-1286/KLF12 axis. Cell Death Dis. 2022 Jul 4;13(7):578. doi: 10.1038/s41419-022-04996-2. PMID: 35787628; PMCID: PMC9253045.
2. Geng L, Liao B, Jin L, Yu J, Zhao X, Zhao Y, Zhong L, Wang B, Li J, Liu J, Yang JK, Jia W, Lian Q, Xu A. β-Klotho promotes glycolysis and glucose-stimulated insulin secretion via GP130. Nat Metab. 2022 May;4(5):608-626. doi: 10.1038/s42255-022-00572-2. Epub 2022 May 12. PMID: 35551509.
3. Xia P, Chen J, Liu Y, Cui X, Wang C, Zong S, Wang L, Lu Z. MicroRNA-22-3p ameliorates Alzheimer's disease by targeting SOX9 through the NF-κB signaling pathway in the hippocampus. J Neuroinflammation. 2022 Jul 12;19(1):180. doi: 10.1186/s12974-022-02548-1. PMID: 35821145; PMCID: PMC9277852.
4. Zhu Z, Cao C, Zhang D, Zhang Z, Liu L, Wu D, Sun J. UBE2T-mediated Akt ubiquitination and Akt/β-catenin activation promotes hepatocellular carcinoma development by increasing pyrimidine metabolism. Cell Death Dis. 2022 Feb 15;13(2):154. doi: 10.1038/s41419-022-04596-0. PMID: 35169125; PMCID: PMC8847552.
5. Walton ZE, Patel CH, Brooks RC, Yu Y, Ibrahim-Hashim A, Riddle M, Porcu A, Jiang T, Ecker BL, Tameire F, Koumenis C, Weeraratna AT, Welsh DK, Gillies R, Alwine JC, Zhang L, Powell JD, Dang CV. Acid Suspends the Circadian Clock in Hypoxia through Inhibition of mTOR. Cell. 2018 Jun 28;174(1):72-87.e32. doi: 10.1016/j.cell.2018.05.009. Epub 2018 May 31. PMID: 29861175; PMCID: PMC6398937.
6. 李晨, 张斌, 王军,等. 慢病毒表达双报告基因载体系统的构建及病毒制备[J]. 中国实验血液学杂志, 2011, 19(6):4.
