4月20-21日,2022第三届CBIC细胞生物产业大会(第三届细胞治疗与再生医学大会暨中国生物医药创新合作大会)在深圳隆重举办,开展近60余场高端峰会,话题涉及“细胞疗法创新与应用”、“3D细胞培养与类器官临床应用”、“细胞外泌体再生与肿瘤免疫技术研发”、“基因治疗与溶瘤病毒”、“新型疫苗、抗体药物开发与靶点筛选”等,行业大咖云集,共话细胞产业和生物医药行业发展。

浙江泰林生物技术股份有限公司(股票代码;300813)受邀出席本次会议,我司细胞工程首席专家韩冰于专题一细胞疗法创新与应用论坛为大家带来《ATMP药物生产的微生物质量控制》的专题报告,受到现场专家、客户、新闻媒体的重点关注。


与传统药物相比前沿治疗药物(ATMP)在研发及生产过程中的产品质量控制面临诸多挑战,例如无法终端灭菌、传统药典中无菌检查方法检测周期长、具有生物活性需要多次QC测试、产量有限QC测试样品量少等。
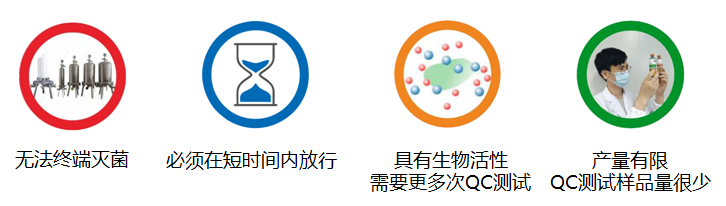
在生物药行业高速发展的背景下,欧盟及美国药典均出台相关规范鼓励和要求使用新技术,来应对前沿治疗药物(ATMP)产品质量控制所面临的挑战。泰林生物经过多年技术积累和持续的研发创新,完成了全自动无菌检查培养系统ASTS系列产品的研发,为前沿治疗药物(ATMP)产品质量控制提供新方法。

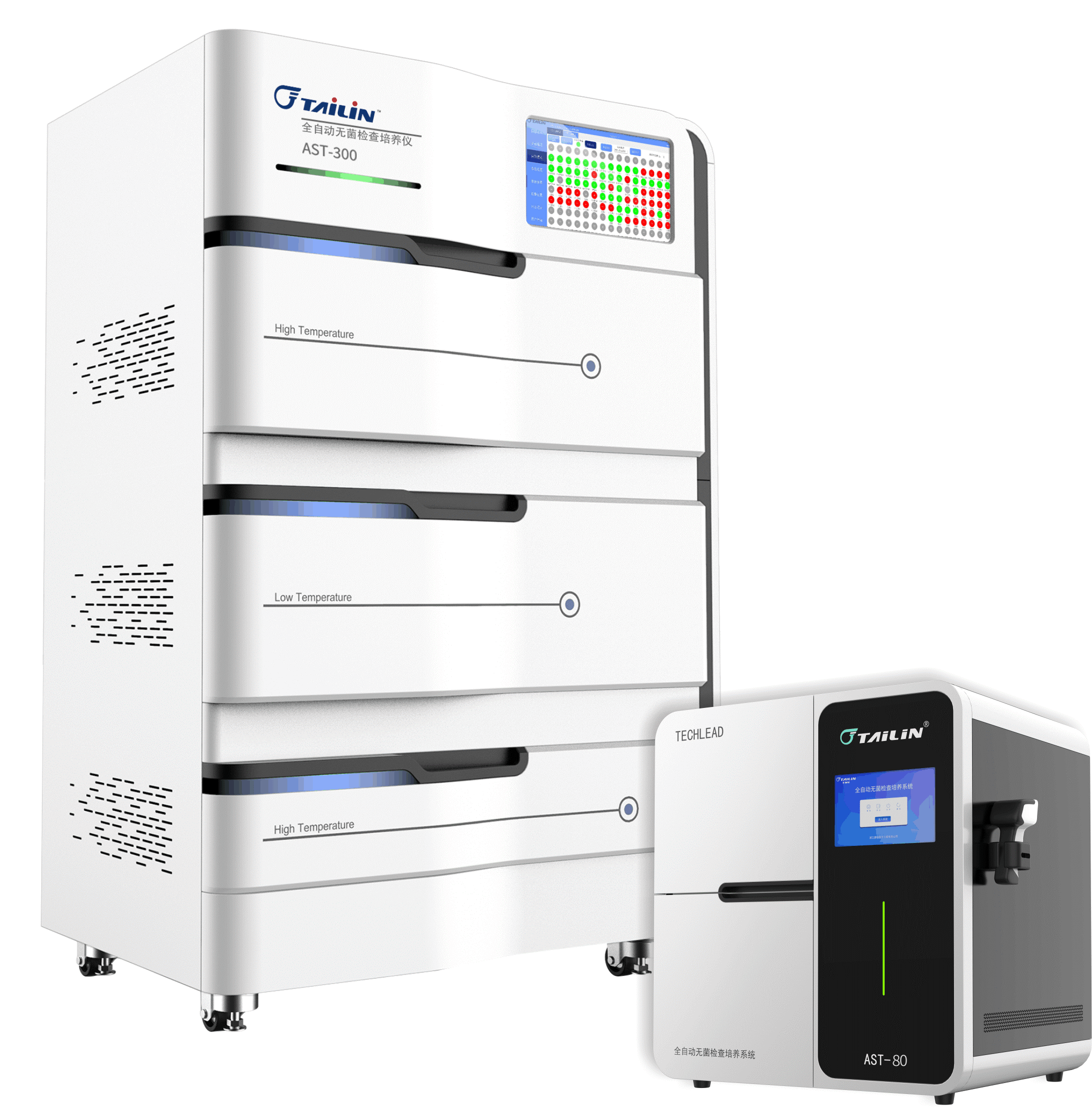
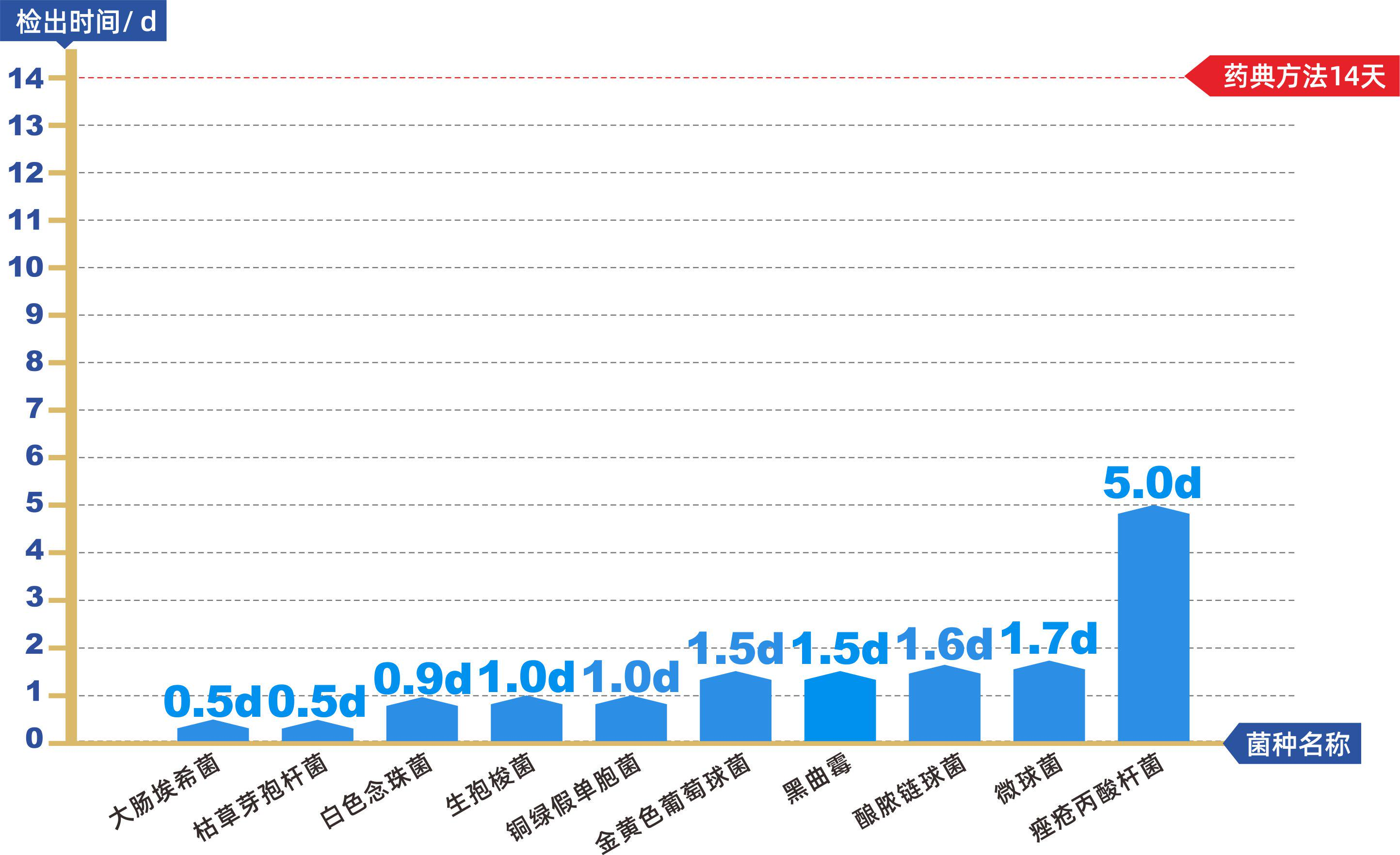
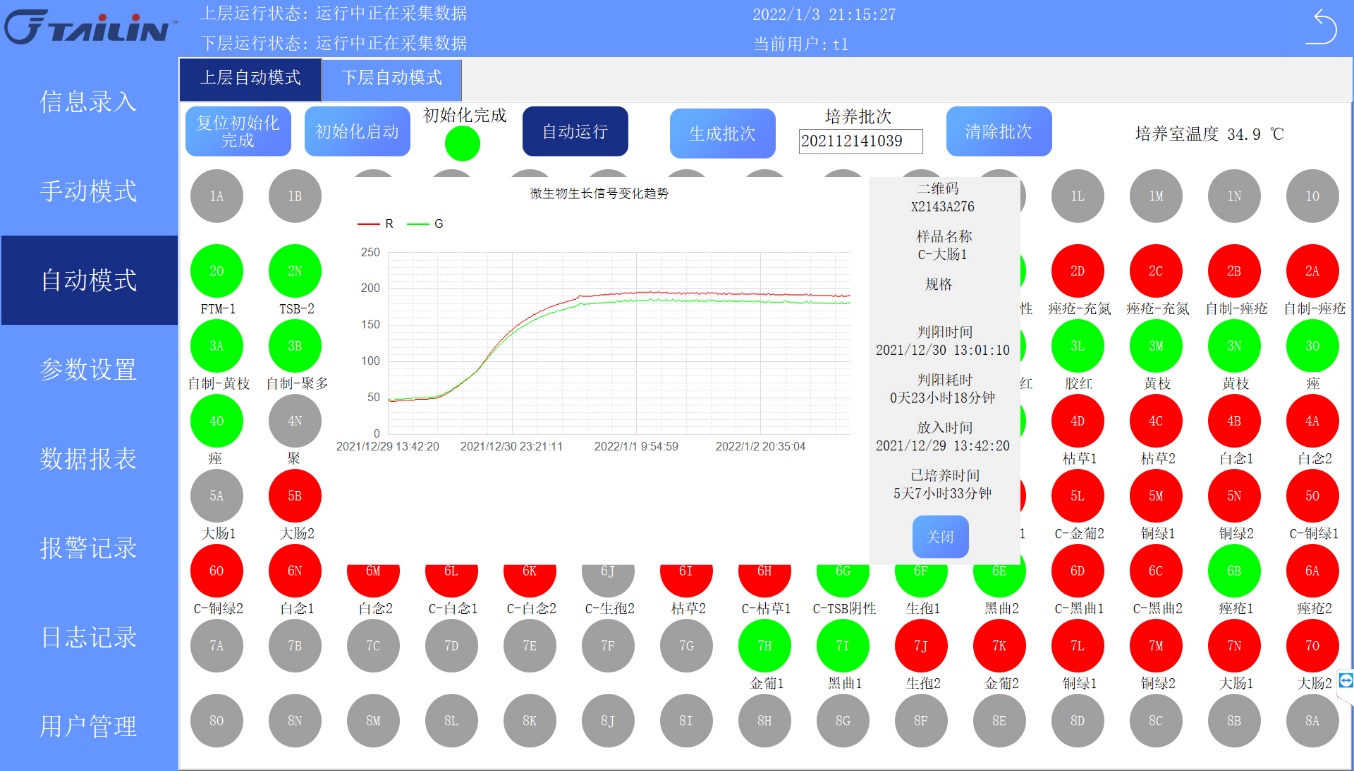
报告中指出,十三五国家重大科技专项成果全自动无菌培养系统AST-300和AST-80是专用于药品快速无菌检查的智能化仪器,由恒温培养箱体,自动化检测单元、培养容器、微生物生长信号感应器等组成。其原理是基于微生物呼吸作用产生的CO₂,引起培养容器上感应器颜色的改变,通过设备的视觉相机连续扫码感应器图像及对应二维码,由计算机系统进行视觉分析并转换为生长信号,根据变化趋势分析及专用的算法来判断无菌检查结果。 全自动无菌检查培养系统ASTS产品核心特点: 具备AST 80、180MF、300多种规格,适配多种用户需求; 多温区设置,每个舱体可单独设置培养温度(温度范围:20°C-40°C),既满足药典要求的30-37度、20-25度培养条件,又可满足其他培养温度的需求; 满足于国家药典委员会于2021年10月26日公示的“通则 细胞类制品微生物检验法”中规定的培养基要求 ; 支持直接接种法和薄膜过滤法; 最快12小时即可获得阳性判读结果(传统无菌检查大于≥14天); 细胞类制品微生物检查法通则草案中规定菌种 灵敏度高,可以检出低污染水平微生物(1-10cfu); 可靠性强,自动判读无菌检查结果; AST-300设备操作界面 实时追溯,全程追踪记录,数据完整性符合GMP要求; 泰林生物作为国内微生物控制与检测行业的领军企业,致力于成为生命科学领域**的系统解决方案提供商,在前沿治疗药物(ATMP)领域已经具备了自动化、智能化、系统化的解决方案,合作客户遍及国内细胞和基因治疗药物企业、CRO/CDMO、科研院校以及医疗机构等单位,为国内生物药研发及产业化发展提供专业的技术支持。 更多精彩,敬请关注细胞和基因药物研发及产业化系列课题研讨会线上直播。