高密度脂蛋白(HDL)的代谢受清道夫受体B组1型(SR-BI)与肝脏多种信号分子之间复杂的相互作用调节。 2023年10月19日,复旦大学徐延勇及首都医科大学李晶共同通讯在Developmental Cell 在线发表题为“Hepatocytic lipocalin-2 controls HDL metabolism and atherosclerosis via Nedd4-1-SR-BI axis in mice”的研究论文,该研究发现脂钙素-2 (Lcn2)是肝脏SR-BI、HDL代谢和动脉粥样硬化的关键调节因子。 在西式饮食喂养的Ldlr-/-小鼠中,肝细胞中人类Lcn2的过表达通过SR-BI减弱了动脉粥样硬化的发展,而肝细胞特异性消融Lcn2则具有相反的效果。机制上,肝细胞Lcn2通过阻断Nedd4 -1介导的SR-BI泛素化K500和K508,改善HDL代谢,减轻动脉粥样硬化。Lcn2改善的HDL代谢在肝细胞特异性Nedd4-1或SR-BI缺失小鼠和SR-BI (K500A/K508A)突变小鼠中被消除。总之,该研究通过阻断Nedd4 -1介导的SR-BI泛素化,确定了从Lcn2到HDL的调控轴,并证明肝细胞Lcn2可能是改善HDL代谢以治疗动脉粥样硬化性心血管疾病的有希望的靶点。

动脉粥样硬化性心血管疾病(ASCVD)仍然是全球发病率和死亡率的主要原因。动脉粥样硬化是一种多因素疾病,具有常见的危险因素,如血脂异常、高血压、糖尿病和肥胖。高密度脂蛋白(HDL)通过促进巨噬细胞逆向胆固醇转运(RCT)来发挥其对ASCVD的动脉粥样硬化保护作用,巨噬细胞通过HDL受体从HDL颗粒中提取胆固醇酯并转移到胆汁中肠排泄。此外,HDL具有其他多种抗动脉粥样硬化作用,包括抗氧化、抗炎症和抗血栓形成。然而,随着全身炎症状态的发生,由于HDL颗粒成分的改变,HDL的功能可能从抗动脉粥样硬化转变为促动脉粥样硬化,导致HDL代谢受损。例如,血清淀粉样蛋白A (SAA)被证明通过改变HDL的抗炎特性及其功能来破坏HDL代谢并加剧动脉粥样硬化。由于HDL颗粒的异质性和HDL代谢的复杂性,到目前为止,控制HDL代谢的治疗靶点仍然知之甚少。哺乳动物清道夫受体B类I型(SR-BI)是一种509个氨基酸,~82 kDa的完整膜糖蛋白,主要表达于肝脏。SR-BI被确立为一种高亲和力HDL受体,在介导肝脏从球形HDL选择性摄取胆固醇酯中起关键作用,从而改善HDL代谢,促进巨噬细胞RCT,降低血浆HDL胆固醇(HDL-C)水平,并阻碍动脉粥样硬化的发展。相反,据报道SR-BI缺乏或SR-BI功能缺失突变会损害HDL代谢,导致RCT减弱,血浆HDL-C水平升高,加速动脉粥样硬化的病理进展。此外,肝脏SR-BI可以调节HDL的组成和HDL的抗炎特性。在Srb1-/-小鼠中,HDL的蛋白质组学谱随着促炎蛋白(如SAA)水平的增加而显著改变。考虑到肝脏SR-BI在HDL代谢和动脉粥样硬化中的关键作用,SR-BI是多功能HDL-based治疗的有效靶点。在临床研究中,作者发现肝脏Lcn2 mRNA水平与血浆HDL-C水平呈较强的负相关,提示Lcn2可能是HDL代谢的重要调节因子。Lcn2是一种25 kda的分泌性糖蛋白,在葡萄糖和甘油三酯代谢中起重要作用,并阻止肥胖、糖尿病和NAFLD的进展。到目前为止,只有一份来自Bot实验室的报告显示Lcn2对实验性动脉粥样硬化具有阶段依赖性,因为Ldlr-/-小鼠中Lcn2的整体消融会增加疾病早期的动脉粥样硬化。然而,肝脏Lcn2在HDL代谢和动脉粥样硬化中的作用是完全未知的。
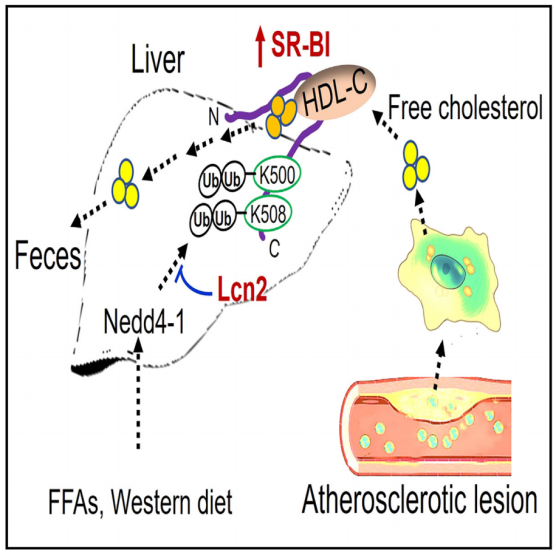
机理模式图(图源自Developmental Cell )
神经前体细胞表达发育下调的4-1(Nedd4-1)是负责蛋白质泛素化的E3连接酶。结构研究表明,Nedd4-1蛋白主要包含3个结构域:C2结构域、WW结构域和HECT(与E6-AP羧基T端同源)结构域。C2结构域可以介导Nedd4-1与膜的结合并参与底物的识别虽然Nedd4-1有许多底物,但Nedd4-1在脂质代谢中的作用却鲜为人知。到目前为止,同一实验室仅有两项研究报道Nedd4-1可以介导ABCG1或ABCG4的泛素化并调节细胞胆固醇输出活性。然而,Nedd4-1是否调节SR-BI翻译后修饰或HDL代谢尚不清楚。该研究发现肝细胞Lcn2通过阻断Nedd4-1介导的SR-BI泛素化位点K500和K508来调节HDL代谢和动脉粥样硬化。该研究通过阻断Nedd4 -1介导的SR-BI泛素化,确定了从Lcn2到HDL的调控轴,并证明肝细胞Lcn2可能是改善HDL代谢以治疗动脉粥样硬化性心血管疾病的有希望的靶点。
和元助力
和元生物有幸为研究者提供实验中使用的AAV病毒载体,以实际行动助力基础科学研究!
| AAV8-TBG-hSrb1 |
| AAV8-TBG-hSrb1 (K500A/K508A) |
| AAV8-TBG-Nedd4-1 |
| AAV8-TBG-Cre |
原文链接:https://doi.org/10.1016/j.devcel.2023.09.007
# END #
// 免责声明
* 文章内容来源于“iNature”公众号,转载文章仅供分享,如有涉及版权问题,请及时与我们联系,我们将给予删除或下线处理。
业务咨询
更多活动详情可咨询(微信/电话):15800353038
